- Startseite >
- Allgemeinerkrankungen >
- Diabetes mellitus
Diabetes mellitus
Allgemeinerkrankungen
Bei der Autoimmunerkrankung Diabetes mellitus Typ 1 kommt es aufgrund einer stetig voranschreitenden Zerstörung der insulinproduzierenden Beta-Zellen in der Bauchspeicheldrüse (Pankreas) zu einem absoluten Insulinmangel. Die Zerstörung wird dabei durch das körpereigene Immunsystem ausgelöst, meist bereits im Kindesalter. Am Anfang der Erkrankung besteht noch eine gewisse Eigenproduktion (Remissionsphase), die mit der Zeit jedoch vollständig erlischt. Der daraus resultierende absolute Insulinmangel erfordert somit eine lebenslängliche externe Insulinzufuhr – mittels Insulinpumpe oder Insulinpen – durch den Patienten. Heute kann über eine Autoantikörper-Bestimmung im Blut das Risiko für einen Diabetes mellitus Typ 1 bestimmt werden, mit der Möglichkeit, den Ausbruch der Krankheit medikamentös hinauszuzögern, bis heute leider aber noch nicht zu verhindern.
Bei Diabetes mellitus Typ 2 reagieren die Körperzellen meist im höheren Lebensalter nicht mehr richtig auf das Insulin (Insulinresistenz)
In beiden Fällen ist zu viel Zucker (Glukose) im Blut, daher auch der Name "Blutzuckerkrankheit".
Der Name Diabetes (griechisch „hindurchfließen") mellitus (lateinisch „honigsüß") beschreibt die Krankheitszeichen, die bereits im Altertum erkannt wurden: starker Durst, häufiger Harndrang und auffallend süßer Urin.
Häufigkeit
Aktuell haben in Deutschland etwa 8,5 Mio. Menschen Typ-2-Diabetes und 32.000 Kinder und Jugendliche sowie 341.000 Erwachsene einen Typ-1-Diabetes. Im Jahr 2040 werden schätzungsweise 11,5 Mio. Menschen die Diagnose Typ-2-Diabetes haben. (Deutscher Gesundheitsbericht Diabetes 2022: Die Bestandsaufnahme, S. 15)
Die Diabetessterblichkeit ist deutlich höher als bisher angenommen. Insbesondere in jüngeren und mittleren Altersgruppen sind die Lebenserwartung und die zu erwartenden gesunden Lebensjahre bei Menschen mit Diabetes geringer.
Habe ich Diabetes? Als Diabetes-(Risiko-)Screening bietet sich der FINDRISK-Fragebogen oder der Deutsche Diabetes Risiko-Test. Die weiterführende Diagnostik muss vom Hausarzt veranlasst werden.
Diabetes & Parodontitis
Parodontitis hat über die Entzündungsprozesse indirekte Effekte auf die Kontrolle des Blutzuckerwertes. Parodontitis & Diabetes mellitus beeinflussen sich dabei gegenseitig. Parodontitis-Therapie hat auch einen positiven Einfluss auf Diabetes mellitus.
Bei gut eingestelltem Diabetes haben Zahnimplantate eine gute Prognose. Erst nach längerer Zeit ist das Risiko für einen Implantatverlust etwas erhöht.
Wechselwirkungen
Parodontitis und Diabetes beeinflussen sich wechselseitig – dieser Zusammenhang ist wissenschaftlich gut erforscht. Über 11 Mio. Menschen in Deutschland hatten im Jahr 2014 eine behandlungsbedürftige Entzündung des Zahnhalteapparates (Parodontitis) – den meisten (ca. 80 %) ist dies selbst gar nicht bewusst.
Im Zusammenhang eines Diabetes mellitus auf das parodontale Erkrankungsgeschehen nehmen sogenannte advanced glycation end products (AGEs) eine Schlüsselrolle ein. Die AGEs entstehen bei der Bindung von z. B. Glukose an freie Aminogruppen von Nukleinsäuren, Lipiden und Proteinen (Hyperglykämie). Docken diese AGEs an spezifische Rezeptoren auf Entzündungszellen (z. B. Makrophagen und Mastzellen) werden Entzündungsmediatoren und matrixabbauende Enzyme freigesetzt. So werden sowohl die Entzündungsvorgänge als auch der Knochenabbau bei der Parodontitis verstärkt. Zudem können AGEs hemmend auf Regenerations- und Wundheilungsprozesse wirken. Bei übergewichtigen oder adipösen Typ-2-Diabetikern können sogenannte Adipokine die parodontalen Entzündungsvorgänge und Knochenabbauprozesse verstärken.
Andererseits beeinflusst die Parodontitis die glykämische Einstellung von Diabetikern. Zirkulierende Entzündungsmediatoren binden verstärkt direkt an Insulinrezeptoren und hemmen so den Glukoseabbau – der Glukosespiegel im Blut steigt.
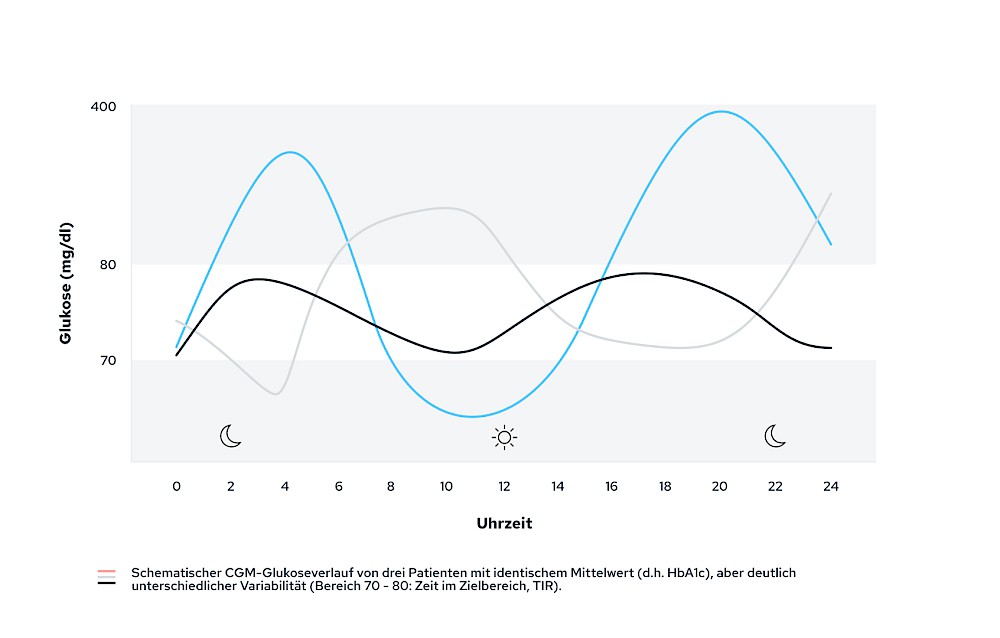 Schematischer CGM-Glukoseverlauf: Unterschiedliche Variabilität bei identischem Mittelwert
Schematischer CGM-Glukoseverlauf: Unterschiedliche Variabilität bei identischem Mittelwert
Symptome
Menschen mit Diabetes mellitus leiden an:
- Vermehrtem Durst und Harndrang
- Mitunter ungewolltem Gewichtsverlust
- Nervenschädigungen und Empfindungsstörungen (Polyneuropathie)
- Schädigung der Blutgefäße – erhöhtes Risiko für Herzinfarkt, Schlaganfall, chronische Nierenerkrankung, Sehverlust
Therapie
Bei Diabetes mellitus Typ 1 sind die Betroffenen lebenslänglich darauf angewiesen, Insulin zu spritzen (alternativ: Insulinpumpe).
Bei Diabetes mellitus Typ 2 kann sich die Insulinresistenz allein durch gesunde Ernährung und Sport wieder abbauen (reversibel). Häufig jedoch sind zusätzlich Medikamente (z. B. Metformin, Insulin) zur Senkung des Blutzuckers nötig.
Metformin ist ein Biguanid und wird aus der französischen Fliederpflanze gewonnen. Es hemmt die Neubildung von Glukose in der Leber, wodurch weniger Zucker ins Blut gelangt. Zudem lässt Metformin die Zellen auf Insulin wieder besser ansprechen. Weiter wird vermutet, dass Metformin durch Wirkung auf den Darm und das Gehirn den Blutzucker verbessert.
Kombitherapie – ein Ansatz für die Zukunft
Ein neuer Ansatz setzt nicht allein auf die Senkung des Blutzuckerspiegels sondern versucht zugleich das sogenannte metabolische Syndrom (Fettleibigkeit – Adipositas) besser in den Griff zu bekommen.
- SGLT2-Inhibitoren
- GLP-1-Rezeptoragonisten
SGLT2-Inhibitoren werden über den Mund eingenommen (z. B. Dapagliflozin, Empagliflozin,, …). Sie bewirken eine vermehrte Ausscheidung von Glukose über die Niere ohne die Gefahr einer Unterzuckerung.
GLP-1-Rezeptoragonisten werden subkutan injiziert (z. B. Exenatid, Liraglutid, …). Sie imitieren die Wirkung des Peptidhormons und Inkretin Glukagon-like Peptid 1 (GLP-1) und helfen so dabei, Übergewicht zu reduzieren. Gleichzeitig führt dies zu einen positiven Effekt auf Blutzucker und Blutdruck. Der Effekt der Kombination beider Wirkstoffe ist mit Insulin zu vergleichen.
Auch über lange Beobachtungszeiträume in verschiedenen Studien sind die Nebenwirkungen (Pilzinfektionen, Übelkeit und Erbrechen) gering, vergehen schnell wieder und lassen sich durch eine Reduktion der Dosis einfach in den Griff bekommen – insgesamt ein vielversprechender Ansatz.
Screening: HbA1c-Wert
Der HbA1c-Wert wird auch als Langzeit-Blutzuckerwert (Blutzuckergedächtnis) bezeichnet und gibt Auskunft über den Verlauf der Blutzuckerwerte in den letzten acht bis zwölf Wochen. Der Wert beschreibt den prozentualen Anteil des roten Blutfarbstoffs (Hamöglobins) in den roten Blutkörperchen (Erythrozyten), der durch Glucose gebunden ist. Diese Bindung wird auch Glykosylierung bezeichnet. Der HbA1c-Wert wird vom Arzt bestimmt
Wie hoch darf der Wert sein?
Nicht-Diabetiker haben einen HbA1c-Wert um die 5 % (30 mmol/mol). Beim Typ-1-Diabetes empfiehlt die Deutsche Diabetes Gesellschaft einen HbA1c-Wert unter 7,5 % (58 mmol/mol). Beim Typ-2-Diabetes werden Zielwerte zwischen 6,5 bis 7,5 % (48 und 58 mmol/mol) empfohlen.
Die genannten HbA1c-Zielwerte sind Richtwerte. Gemeinsam mit dem Arzt erfolgt eine individuelle Festlegung, die die persönlichen Lebensumstände des Patienten, sein Alter und mögliche Begleiterkrankungen berücksichtigen.
Gerade im hohen Alter gelten teilweise andere Regeln. Bei Senioren mit einem hohen Sturzrisiko werden höhere Blutzuckerwerte toleriert, um Unterzuckerungen zu vermeiden und damit das Sturz- sowie das Verletzungsrisiko zu senken. Zudem schüttet der Körper bei Unterzuckerung vermehrt Adrenalin aus, wodurch das Risiko für Herzrhythmusstörungen oder einen Infarkt steigt.
Eine konsequente Parodontitistherapie kann bei Typ-2-Diabetikern den HbA1c-Wert um 0,4 % senken.
Allerdings hat der HbA1c-Wert mehrere Einschränkungen:
- Es handelt sich nur um einen Durchschnittswert der letzten 2 bis 3 Monate;
- Im täglichen Diabetes-Management keine Aussage zu Unterzuckerung bzw. Überzuckerung
- Unzuverlässig bei bestimmten Grundkrankheiten sowie während der Schwangerschaft
- Ethnische Unterschiede
- Keine Informationen zur Anpassung des Behandlungsschemas bei erhöhten Werten
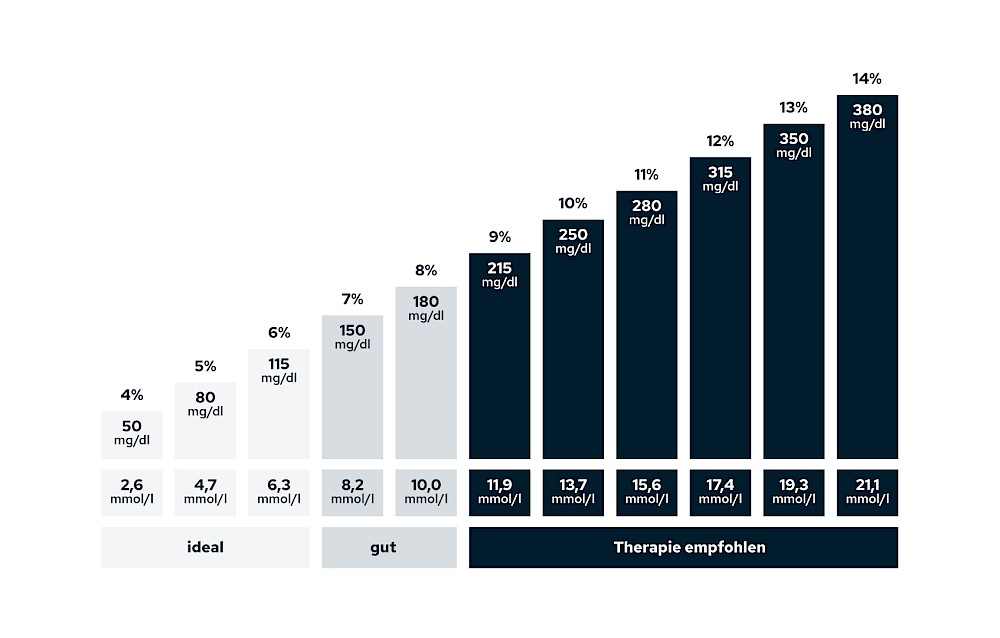 Therapieempfehlung bei erhöhtem HbA1c-Wert
Therapieempfehlung bei erhöhtem HbA1c-Wert
Screening: Time in Range
Verfahren zur kontinuierlichen Glukose-Messung (CGM – continous glucose monitoring) erlauben mit der Time in Range (TIR) die Feststellung der Zeit, in der sich die Blut-Glukose-Werte in einem vorab definierten Zielkorridor befindet.
Während das HbA1c den Mittelwert der Blutzuckerkontrolle über lange Zeiträume (Wochen bis Monate) reflektiert, spiegelt die TIR das Maß der Glukosevariabilität über einen oder mehrere Tage wider. Für die Beurteilung der Blutzucker-Einstellungsqualität sollten daher sowohl der HbA1c als auch die TIR herangezogen werden.
Als Zielkorridor werden 70 bis 180 mg/dl (3,9 bis 10,0 mmol/l) definiert. Wird der Zielkorridor überschritten, steigt das Risiko für Hyperglykämien und damit auch für eine diabetische Ketoazidose. Wird der Zielkorridor unterschritten, steigt das Risiko für Hypoglykämien. Je niedriger die TIR, desto stärker die Glukosevariabilität und desto höher die Gefahr von hypo- und hyperglykämischen Komplikationen. Wissenschaftliche Untersuchungen konnten einen Zusammenhang zwischen einer erhöhten Glukosevariabilität (bzw. niedriger TIR) und diabetesassoziierten Komplikationen wie Retinopathie, Mikroalbuminurie und Neuropathien feststellen.

Diese Seite wurde zuletzt am 23.07.2024 geändert.